АТФ в бодибилдинге
Содержание
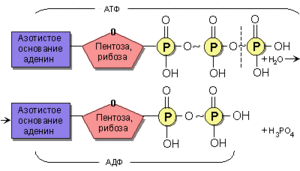
АТФ должна пройти через несколько ступеней, чтобы дать нам энергию. Сначала при помощи специального коэнзима отделяется один из трёх фосфатов (каждый из которых даёт десять калорий), высвобождается энергия и получается аденозин дифосфат (АДФ). Если энергии требуется больше, то отделяется следующий фосфат, формируя аденозин монофосфат (АМФ). Главным источником для производства АТФ служит глюкоза, которая в клетке инициально расщепляется на пируват и цитозол.
Во время отдыха происходит обратная реакция – при помощи АДФ, фосфагена и гликогена фосфатная группа вновь присоединяется к молекуле, формируя АТФ. Для этих целей из запасов гликогена берётся глюкоза. Вновь созданный АТФ готов к следующему использованию. В сущности АТФ работает как молекулярная батарея, сохраняя энергию, когда она не нужна, и высвобождая в случае необходимости.
Структура АТФ [ править | править код ]
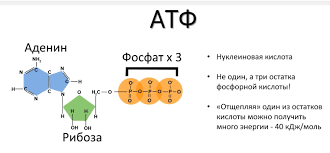
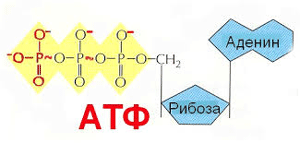
Молекула АТФ состоит из трёх компонентов:
1. Рибоза (тот же самый пятиуглеродный сахар, что формирует основу ДНК)
2. Аденин (соединённые атомы углерода и азота)
3. Трифосфат
Молекула рибозы располагается в центре молекулы АТФ, край которой служит базой для аденозина. Цепочка из трёх фосфатов располагается с другой стороны молекулы рибозы. АТФ насыщает длинные, тонкие волокна, содержащие протеин, называемый миозином, который формирует основу наших мышечных клеток.
Системы АТФ [ править | править код ]
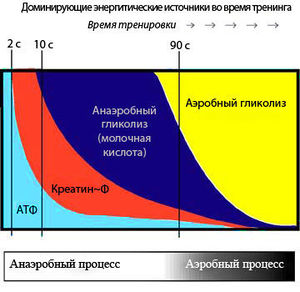
Запасов АТФ достаточно только на первые 2-3 секунды двигательной активности, однако мышцы могут работать только при наличии АТФ. Для этого существуют специальные системы, которые постоянно синтезируют новые молекулы АТФ, они включаются в зависимости от продолжительности нагрузки (см. рисунок). Это три основные биохимические системы:
1. Фосфагенная система (Креатин-фосфат)
2. Система гликогена и молочной кислоты
3. Аэробное дыхание
Фосфагенная система [ править | править код ]
Когда мышцам предстоит короткая, но интенсивная активность (приблизительно 8-10 секунд), используется фосфагенная система – АДФ соединяется с креатина фосфатом. Фосфагенная система обеспечивает постоянную циркуляцию небольшого количества АТФ в наших мышечных клетках. Мышечные клетки также содержат высокоэнергетический фосфат – фосфат креатина, который используется для восстановления уровня АТФ после кратковременной, высокоинтенсивной работы. Энзим креатин киназа отнимает фосфатную группу у креатина фосфата и быстро передаёт её АДФ для формирования АТФ. Итак, мышечная клетка превращает АТФ в АДФ, а фосфаген быстро восстанавливает АДФ до АТФ. Уровень креатина фосфата начинает снижаться уже через 10 секунд высокоинтенсивной активности. Пример использования фосфагенной системы энергоснабжения – это спринт на 100 метров.
Система гликогена и молочной кислоты [ править | править код ]
Система гликогена и молочной кислоты снабжает организм энергией медленнее, чем фосфагенная система, и предоставляет достаточно АТФ примерно для 90 секунд высокоинтенсивной активности. В ходе процесса из глюкозы мышечных клеток в результате анаэробного метаболизма происходит формирование молочной кислоты.
Учитывая тот факт, что в анаэробном состоянии организм не использует кислород, эта система даёт кратковременную энергию без активации кардио-респираторной системы точно так же, как и аэробная система, но с экономией времени. Более того, когда в анаэробном режиме мышцы работают быстро, они очень мощно сокращаются, перекрывая поступление кислорода, так как сосуды оказываются сжатыми. Эту систему ещё можно назвать анаэробно-респираторной, и хорошим примером работы организма в этом режиме послужит 400-метровый спринт. Обычно продолжать работать таким образом атлетам не даёт мышечная болезненность, возникающая в результате накопления молочной кислоты в тканях.
Аэробное дыхание [ править | править код ]
Если упражнения длятся более двух минут, в работу включается аэробная система, и мышцы получают АТФ вначале из углеводов, потом из жиров и наконец из аминокислот (протеинов). Протеин используется для получения энергии в основном в условиях голода (диеты в некоторых случаях). При аэробном дыхании производство АТФ проходит наиболее медленно, но энергии получается достаточно, чтобы поддерживать физическую активность на протяжении нескольких часов. Это происходит, потому что глюкоза распадается на диоксид углерода и воду беспрепятственно, не испытывая противодействия со стороны, например, молочной кислоты, как в случае анаэробной работы.
Коротко и простым языком про молекулы АТФ
Что оно такое – молекулы АТФ?!
В наших клетках происходят различные энергетические процессы: запасание и использование энергии, ее трансформация и высвобождение. Кажется невероятным, что какая-то абстрактная энергия вдруг может преобразовываться и создавать другие молекулы, выполняя при этом полезную работу для организма.
Для справки: АТФ (аденозинтрифосфат) – молекула, которая выполняет роль источника энергии для всех процессов в организме, в том числе, и для движения. Открыта эта молекула была в 1929 году. Главным источником для производства молекулы АТФ служит глюкоза.
По сути, молекула АТФ – это своеобразная молекулярная батарея, которая сохраняет энергию в те моменты, когда она не используется, и потом высвобождает энергию при необходимости организма.
Структура и формула энергетических молекул
При расщеплении молекулы АТФ происходит сокращение мышечного волокна, из-за чего выделяется энергия, позволяющая мышцам сокращаться.
Для того чтобы дать организму энергию АТФ проходит несколько этапов. В процессе каждого этапа вырабатывается большее количество энергии, но всегда то, которое затребовано самим организмом.
Главный источник для выработки АТФ — это глюкоза, которая расщепляется в клетках. Молекулы АТФ насыщают энергией длинные волокна мышечных тканей, которые содержат протеин — миозин. Именно так формируются мышечные клетки.
Когда наш организм отдыхает – цепочка процессов преображения молекулы АТФ идёт в обратную сторону. И в этих целях также задействована глюкоза. Созданные молекулы АТФ будут вновь использоваться, как только это станет необходимо организму.
Когда созданная молекулами энергия не нужна, она сохраняется в организме и высвобождается тогда, когда это потребуется.
Молекулы АТФ синтезируют три основные биохимические системы:
– Система гликогена и молочной кислоты
Что это дает нашему организму?!
Фосфагенная система – будет использоваться когда мышцы работают недолго, но очень интенсивно (порядка 10 секунд). Благодаря этой системе происходит постоянная циркуляция небольшого количества молекул АТФ в мышечных клетках. Такой энергии хватит на короткий забег или интенсивную силовую нагрузку в бодибилдинге.
Гликоген и молочная кислота — снабжают энергией организм медленнее, чем предыдущая система. Используется энергия АТФ, которой может хватить на полторы минуты интенсивной работы. В анаэробном режиме мышцы сокращаются крайне мощно и быстро. Именно благодаря этой системе можно пробежать 400 метров спринтерского бега или рассчитывать на более длительную интенсивную тренировку в зале. Но долгое время так работать не позволит ощущение боли в мышцах, которая появляется из-за переизбытка молочной кислоты.
Аэробное дыхание — эта система включается, если тренировка продолжается более двух минут. Тогда мышцы начинают получать энергию молекул АТФ из углеводов, жиров и протеинов. В этом случае АТФ синтезируется медленно, зато энергии хватает надолго — физическая активность может продолжаться несколько часов. Это происходит благодаря тому, что глюкоза распадается без препятствий, у неё нет никаких сторонних противодействий — как препятствует молочная кислота в предыдущем анаэробном процессе.
Роль АТФ в организме
После описания синтеза трех биохимических систем становится понятно, что основная роль АТФ в организме — это обеспечение энергией всех многочисленных биохимических процессов и реакций организма.
То есть большинство энергозатратных процессов у живых существ происходит благодаря АТФ.
Но кроме этого молекула АТФ играет важную роль в синтезе нуклеиновых кислот, регулирует различные биохимические процессы, передает гормональные сигналы клеткам организма и другое.
Вместо выводов
Итак, АТФ – это молекула, которая даёт энергию всем процессам, происходящим в организме, в том числе, она даёт энергию для движения.
Важная роль АТФ в организме и жизни человека доказана не только учёными, но и многими спортсменами, бодибилдерами, фитнес-тренерами. Понимание важности этого вопроса помогает сделать тренировки более эффективными и правильно рассчитать свои физнагрузки.
Для всех, кто занимается силовыми тренировками в зале, фитнесом, бегом и другими видами спорта, нужно понимать и помнить – какие блоки упражнений необходимо выполнять в то или иное время тренировки. Благодаря этому можно откорректировать форму фигуры, проработать мышечную структуру, снизить лишний вес и добиться других улучшающих результатов для своего организма.
Простыми словами о молекулах АТФ
Простыми словами о молекулах АТФ
Из школьного курса биологии мы помним, что молекулы АТФ образуют энергию, которая необходима каждому человеку. Но на страницах учебника были сплошные формулы и пугающие термины, поэтому эта тема прошла мимо нашего внимания. А молекулы АТФ крайне важны, особенно в эпоху, когда вокруг растет количество тренажерных залов.
Любое действие, будь это шаг или дыхание, требует энергетических затрат. Вот только запасов АТФ в организме совсем не много. Исследования показали, что в отдельный момент вес этих молекул составляет около 250 грамм. Этого количества будет недостаточно даже для простой прогулки по лесу. Откуда же берутся молекулы АТФ, чтобы наполнять наш организм энергией?
Что такое АТФ
Аденозинтрифосфорная кислота это вещество, которое чаще других обновляется в организме. Продолжительность жизни АТФ не более минуты. Поэтому она постоянно рождается и распадается. Так происходит в среднем 3000 раз за сутки. Удивительно, но такое количество обновлений составляет 40 кг. Настолько велика потребность человека в энергии.
Этот нуклеотид состоит из трех компонентов:
Молекула АТФ дает энергию для всех процессов, происходящих в организме. Благодаря ее расщеплению сокращаются мышечные волокна. Прежде чем АТФ произведет энергию, она проходит несколько этапов. В процессе расщепления от нее отделяются остатки фосфорной кислоты. Отрыв одной молекулы сопровождается выбросом энергии. Когда отделяется одна молекула фосфорной кислоты, образуется АДФ (аденозиндифосфат), две – АМФ (аденозинмонофосфат).
Синтез молекулы АТФ у человека и животного происходит в митохондриях. Топливом для синтеза выступает глюкоза. Когда запасы гликогена на исходе, начинают задействоваться жировые ресурсы. Спортсмены знают, что для расхода жировых запасов требуются аэробные нагрузки. К ним относятся бег, ходьба, пешие прогулки, катание на коньках и другие.
Роль АТФ в организме
Главная функция аденозинтрифосфорной кислоты – энергетическая. Но она также отвечает за ряд других процессов организме.
Функции АТФ:
Как увеличить выработку АТФ
Количество молекул «энергетической» кислоты зависит от количества митохондрий в организме. Есть несколько способов повысить число митохондрий:
Безусловно, организм сам знает, когда выделять нужные ему вещества. Но если вы регулярно занимаетесь спортом или желаете отсрочить наступление старости, то вам стоит ему немного помочь.
Вторая жизнь АТФ: от главной батарейки до нейромедиатора
Микроглия, которая поддерживает работоспособность нервной системы, да и сами нейроны, вовсю экспонируют некие рецепторы. Активатором для них служит АТФ.
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Все знают АТФ. Но чем занимается АТФ вне клетки? Во что вылилась «пуримагическая гипотеза»? Каким образом клеточное «топливо», синтезируемое в организме буквально килограммами, становится тонким нейромедиатором? Какие клеточные рецепторы могут разрушать наш организм? Обо всём этом вы узнаете из данной статьи.
Конкурс «Био/Мол/Текст»-2020/2021

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Вездесущий АТФ
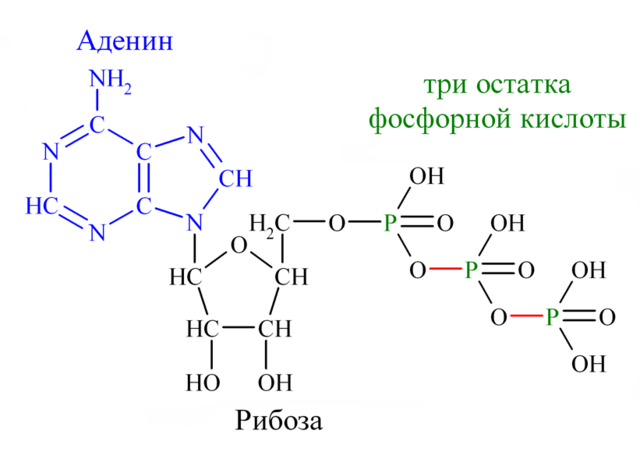
Аденозинтрифосфат (АТФ; рис. 1) — это одна из самых важных молекул в нашем организме. Чаще всего АТФ рассматривается как универсальное топливо для многочисленных «молекулярных машин» и реакций в наших клетках. АТФ одна из самых реакционноспособных молекул на планете. Без него сама жизнь в том виде, в котором она есть сейчас, была бы невозможна.
Рисунок 1. Аденозинтрифосфат (АТФ) — «батарейка» всех клеточных процессов, состоящая из пуринового основания аденина, сахара рибозы и трех остатков фосфорной кислоты, которые хранят в своих связях внушительное количество потенциальной энергии.
Изначально его источником служил лишь бескислородный процесс гликолиза в цитоплазме. Такой способ оказался довольно неэффективным и мог снабжать энергией лишь доядерных прокариот. Появление в клетках верных вассалов-митохондрий позволило вывести производство АТФ на качественно новый уровень и получать его в недостижимых ранее количествах. В митохондриях это происходит при помощи цикла Кребса. Благодаря окислительному фосфорилированию, протекающему в этих органеллах, и клеточному дыханию возникло всё наблюдаемое нами многоклеточное биоразнообразие. Поэтому АТФ в клетках стало много, а за сутки общее количество расходуемого и вновь синтезируемого вещества в нашем теле исчисляется килограммами. Подробнее про синтез АТФ и появление митохондрий можно прочитать на «Биомолекуле» [1].
Более удивительным оказалось то, что и молекула АТФ, и «топливные отходы», получающиеся в результате разрыва фосфатных связей (энергия которых и используется клетками живых организмов для поддержания своей жизнедеятельности), являются частью обширного сигнального аппарата. Эта древняя система сигнализации охватывает весь организм и запускает сложные, порой необратимые, клеточные процессы. Она сообщает нам, когда идти спать, и она же заставляет нас кричать от боли. Находясь на службе клеточного иммунитета, она может как спасти организм от инфекции, так и привести к гибели клеток, став причиной множества воспалительных заболеваний. Более того, АТФ напрямую участвует в регуляции нашей нервной деятельности и служит эффективным нейромедиатором. Однако далеко не сразу эта функция стала очевидной. Для этого потребовались годы усердной работы и исключительное упрямство одного исследователя.
История одного открытия
Люди всегда будут критиковать. Прислушивайся к каждому возражению и проверяй его на практике. И если вдруг окажешься неправ, то ты должен быть первым, кто об этом объявит!
Ульф фон Эйлер,
лауреат Нобелевской премии по физиологии или медицине 1970 г.
Началось всё с того, что в начале 1960-х годов британский ученый-нейробиолог Джеффри Бёрнсток (рис. 2) совершил открытие [2].
Рисунок 2. Джеффри Бёрнсток (1929–2020 гг.). Человек, который своими исследованиями подарил АТФ новую жизнь.
Пребывая в Австралии, Бёрнсток исследовал возбуждение гладкой мускулатуры кишечника морской свинки при помощи электрического тока. Можете не волноваться, он работал на срезе ткани, а не на живой свинке. В то время появились новые электрохимические методы, освоив которые, ученому не терпелось перейти к практике. Ему стало интересно проверить, как гладкая мускулатура будет реагировать на ток в условиях полной блокировки всех известных нервных рецепторов в конкретном срезе ткани. Частая практика у нейробиологов — заблокируй лишние рецепторы нейротоксинами, которыми нас снабдила сама эволюция в лице ядовитых растений и животных (ну и заодно химиков-синтетиков), а потом спокойно изучай то, что осталось рабочим.
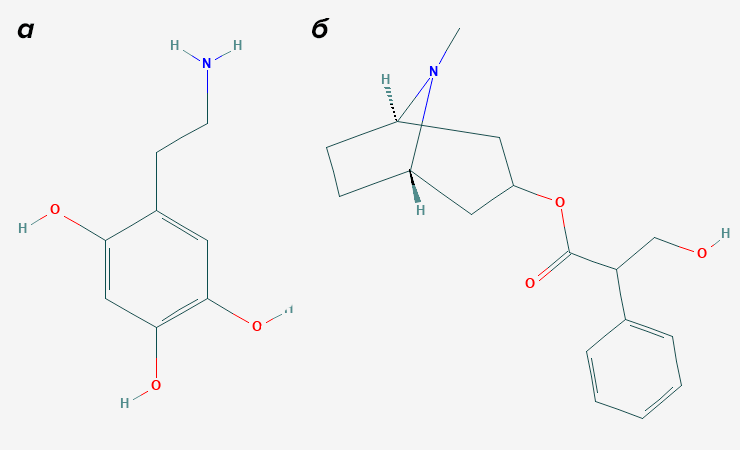
Для начала он обработал ткань 6-гидроксидофамином (рис. 3а). Это синтетический нейротоксин, который нарушает работу дофаминовых и адренергических рецепторов. Затем нужно было заблокировать второй известный тип рецепторов — ацетилхолиновые. Для этого он накачал ткани атропином (рис. 3б), чтобы наверняка отключить все холинорецепторы.
Рисунок 3. Блокаторы Бёрнстока. а — 6-гидроксидофамин (он же 6-OHDA). б — Атропин — растительный алкалоид, известный блокатор ацетилхолиновых рецепторов.
Далее он ввел электрод и простимулировал ткани коротким электрическим импульсом. Ожидалось, что гладкая мускулатура неотвратимо сократится под действием электричества, однако ничего подобного не произошло. Какая-то неведомая сила противодействовала импульсам тока и запускала процессы, мешающие сокращению. На записях электрических сигналов наблюдалась выраженная гиперполяризация, а мышцы расслаблялись даже при серии таких импульсов.
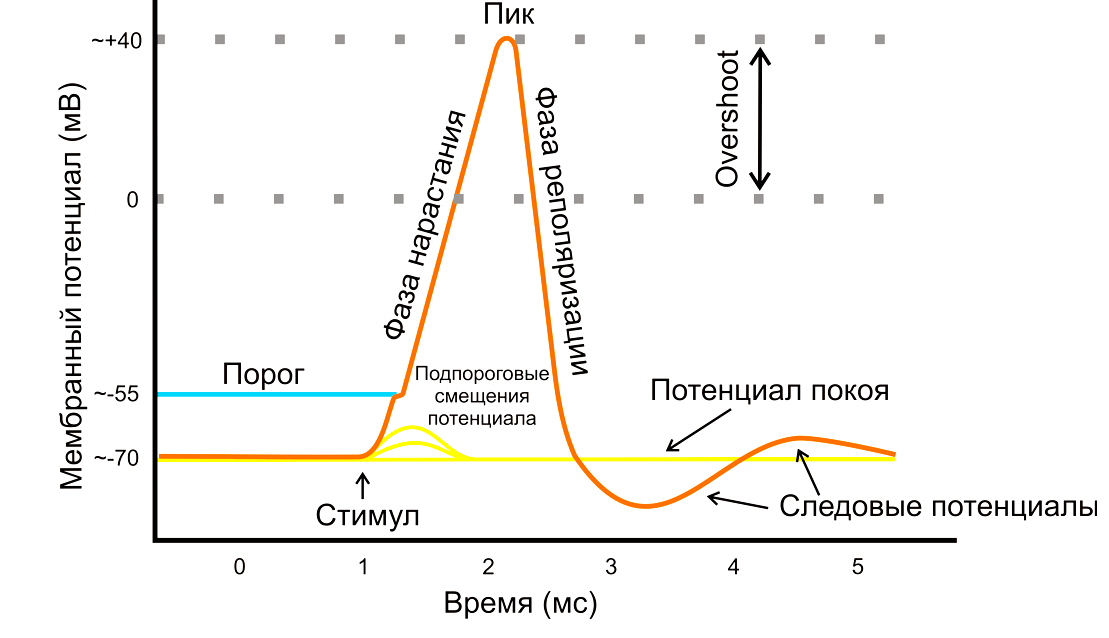
Про потенциал действия
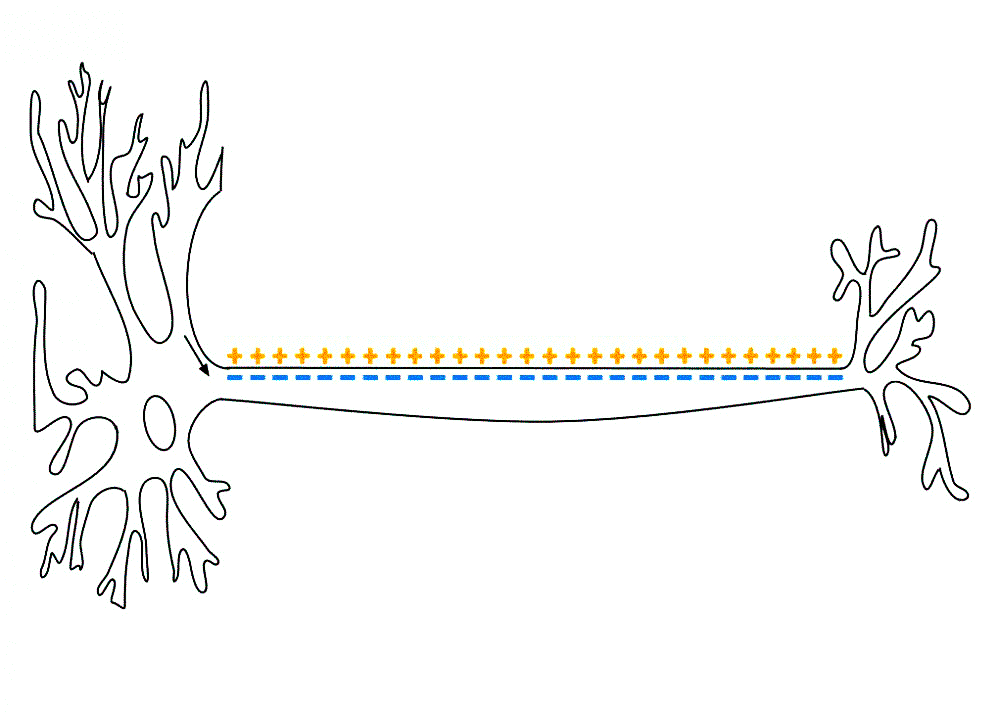
Дело в том, что при потенциале покоя [72] поверхность клеточной мембраны нейрона внутри и снаружи заряжена по-разному: внутри отрицательно, а снаружи положительно. При закачке положительных ионов в клетку, таких как кальций и натрий, потенциал внутренней поверхности мембраны начинает смещаться в положительную сторону и стимулирует нервное возбуждение (рис. 4). «Полюса» начинают двигаться навстречу друг другу, приводя к так называемой деполяризации, пока не достигнут порогового положительного значения. Надо сказать, что существуют тормозящие ионные каналы, которые впускают в клетку отрицательные ионы (хлора, например), либо выпускают наружу положительные (калий). Также есть рецепторы, которые не дают выделяться нейромедиаторам возбуждения. Проще говоря, всячески препятствуют деполяризации мембраны.
Рисунок 4а. Потенциал действия. Нервная клетка, проводящая потенциал действия по аксону.
Рисунок 4б. Потенциал действия. Схема активации потенциала действия. Подробнее о потенциале действия и методах изучения нервной системы можно прочесть в статье «12 методов в картинках: нейробиология» [3].
Такое перетягивание каната позволяет сформировать адекватный ответ на стимул и определяет конечную «положительность» заряда внутренней поверхности мембраны. Потенциал действия работает по принципу «всё или ничего». Только достигнув некоего внутреннего положительного порога, мембрана нейрона волнообразно передает потенциал действия к месту назначения и снова становится отрицательной (фаза реполяризации). Однако то, чем смещать разницу потенциалов на мембране и передавать по нервам потенциал действия, — электрическим током или входом заряженных ионов, — не имеет значения. Именно поэтому мышцы сокращаются и под действием электрического разряда, прямо как в фантастическом романе о монстре Франкенштейна. Процессом, обратным деполяризации, является гиперполяризация, при которой потенциал действия невозможен. Именно ее и наблюдал Бёрнсток в своем эксперименте.
На его счастье, в тот момент Бёрнсток работал с аспирантом из Японии, который использовал свои связи на родине и достал для исследователя знаменитый тетродотоксин (рис. 5а) из рыбы фугу (рис. 5б). Более подробно про тетродотоксин и с чем его едят, можно узнать, прочитав статью, опубликованную на «Биомолекуле» моим однокурсником: «Тетродотоксин — история элегантного убийцы» [4]. Вкратце, этот токсин известен тем, что может блокировать нервную проводимость и как пробка затыкать натриевые каналы. Однако он не лишает гладкую мускулатуру способности сокращаться. Смертоносное вещество было также принято Бёрнстоком в работу.
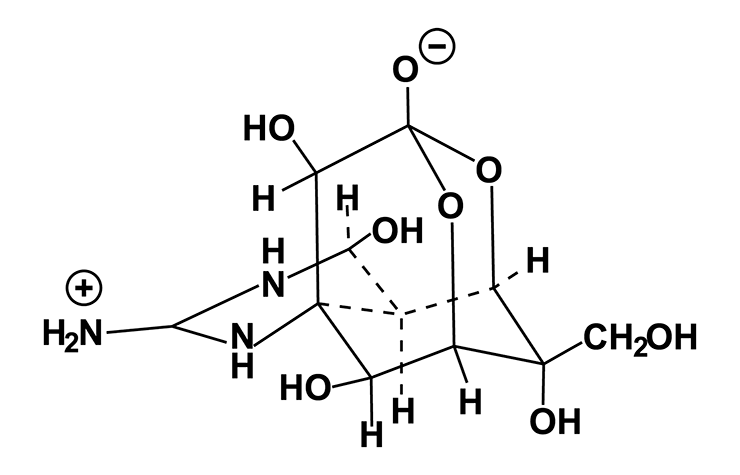
Рисунок 5а. Остолбеней! Структура тетродотоксина довольно уникальна по своей природе. Благодаря положительному заряду гуанидиновая группа ловко маскируется под гидратированные ионы натрия и проникает в пору натриевого канала. Однако за ней идет объемная клетка, сшитая из атомов углерода и кислорода, и утыканная гидроксильными группами. Она накрепко застревает в лоне ионного канала, препятствуя ходу ионов.
Рисунок 5б. Остолбеней! Рыба фугу — самый известный источник тетродотоксина. Однако виной всему не сама рыба, а обитающие в ней бактерии-симбионты. Именно они служат поставщиками яда в ее органах. Фугу считается экстремальным деликатесом в Японии, а для права ее приготовления повару требуется специальная лицензия. Остаточные дозы тетродотоксина в мясе все еще способны вызвать онемение губ и языка у отъявленных гурманов.
После его применения реакция на электрический разряд наконец стала такой, какой ожидалось — гиперполяризация пропала, а мышцы сократились. Вывод был очевиден: в нервах гладкой мускулатуры кишечника присутствовали неизвестные рецепторы (не холинергические и не адренергические), которые противодействовали сокращению и выполняли функции, тормозящие нервный импульс [5]. Начался усиленный поиск вещества, которое могло бы служить активатором этих новых загадочных рецепторов. К поиску применялся ряд стандартных критериев, таких как:
Однако испробованные нейропептиды, моноамины и аминокислоты не удовлетворяли заданным критериям. Как это часто бывает, подсказки лежали под ногами — следовало лишь немного покопать. Дело в том, что задолго до работы Джеффри Бёрнстока множество ученых уже натыкались на странное воздействие внеклеточных пуринов (гетероцикл пурина служит основой для аденозина в молекуле АТФ) на сердечную мышцу и кровеносные сосуды, но не придали этому большого значения. Например, знаменитый биохимик Альберт Сент-Дьердьи (рис. 6а) — тот самый, что впервые выделил витамин С (одновременно с Чарльзом Кингом), — также провел ряд фундаментальных исследований мышечного сокращения. В своей работе 1929 года Сент-Дьерди отметил, что введение пуриновых соединений в кровь животным влияло на их сердечный ритм [6]. Позже Памела Холтон (рис. 6б) в 1959 году замечала, что АТФ выделяется при стимуляции нервов в ушных артериях кролика и ведет к расслаблению стенок сосудов [7]. Однако никто из них не пошел в своих рассуждениях дальше и не узнал, насколько глубока эта кроличья нора.
Рисунок 6. Исследователи, работы которых помогли Джеффри Бёрнстоку отыскать новый нейромедиатор. Альберт Сент-Дьёрдьи (а) и Памела Холтон (б).
Вооружившись этими знаниями и проведя ряд опытов, Бёрнсток со своим коллегой Дэвидом Сэтчеллом доказали, что АТФ действительно активирует как стимулирующие, так и тормозящие эффекты в разных типах тканей организма. Статья об этом вышла в 1970 году [8]. Тем более, тогда уже стало известно о внеклеточных ферментах, способных расщеплять АТФ. Ничего не оставалось, кроме как признать, что аденозинтрифосфат является тем самым нейромедиатором и выдвинуть гипотезу о пуринергической передаче сигнала. Слово «пуринергическая» придумал сам Бёрнсток. Рецепторы, связанные с этим типом передачи сигнала, позже стали называть «пуринергическими», или «пуринорецепторами». Вернувшись в Англию, ученый столкнулся с недоверием со стороны коллег. В то время также был популярен так называемый принцип Дейла. Этот принцип Бёрнсток и многие другие нейробиологи того времени трактовали как утверждение, что один нейрон может осуществлять передачу сигнала при помощи только одного нейротрансмиттера (например ацетилхолина) и уж никак не при помощи нескольких разных. Тем более, при помощи АТФ. К слову, сам Генри Дейл имел в виду немного другое, но кто его слушал. Всем казалось маловероятным, что вездесущая молекула, источник энергии клеток, может участвовать в тонких процессах регуляции нервной деятельности.
Рисунок 7. Джеффри Бёрнсток. Фотография сделана в 1970 году в Мельбурне — как раз в тот год, когда была опубликована его первая статья о роли АТФ в качестве нейромедиатора.
В 1972 году вышла большая обзорная статья с выдвинутой ученым гипотезой о пуринергических нейротрансмиттерах и их возможной совместной трансмиссии с другими рецепторами нейронов (долой принцип Дейла!) [9]. Эта статья вызвала большой резонанс и стала причиной множества дебатов. Ее можно смело назвать кульминацией сделанных Бёрнстоком открытий в рамках его концепции о пуринергической передачи сигнала. В ней Бёрнсток также сетовал, что результаты его работ списывают на артефакты и ошибки эксперимента. Гипотеза Джеффри продолжала получать сопротивление в научных кругах на протяжении почти двух десятков лет. Некоторые оппоненты заявляли, что посвятят жизнь разрушению «пуринергической теории». Уважаемые ученые спорили до хрипоты, а один и вовсе назвал Бёрнстока «изобретателем пуримагической гипотезы» [2].
Но исследователь не сдавался и упрямо продолжал работу. Следующим шагом предстояло выяснить, что же собой представляют рецепторы, которые могут активироваться сигнальными молекулами АТФ, либо продуктами его распада (АТФ → АДФ → АМФ → аденозин → аденин).
Когда я говорю «семейство рецепторов», имеется в виду то, что раньше (в эволюционно древние времена) они кодировались одним геном, но в результате генетической дупликации возникли его видоизмененные копии, благодаря которым появилось разнообразие родственных рецепторов. Такие белки обычно объединяются в одно семейство и сохраняют высокое сходство последовательности и структурной укладки, но могут выполнять разные функции. Это разнообразие особенно велико, если ген белка — ключевой в выживании и эволюции вида при естественном отборе. Например, яды актиний, змей и пауков накопили целые комбинаторные библиотеки из многочисленных видоизмененных копий одного гена какого-нибудь пептидного токсина (который ранее вообще мог исполнять роль протеазного ингибитора, а не молекулярного оружия). Происходило это в результате эволюционного поиска и адаптации яда к своим жертвам, устойчивость которых тоже не стояла на месте в процессе эволюции. Подробнее про это читайте в статьях «Великому комбинатору и не снилось: комбинаторика токсинов пауков» [11] и «Яды — высокоточное оружие: компьютерное исследование природных нейротоксинов» [12]. Разнообразие же родственных пуринорецепторов у млекопитающих обусловливается усложнением организма и нервной системы в целом.
Это деление на семейства было условным и сделано исключительно по фармакологическим показателям. Рецепторы семейства P1 блокировались метилксантинами и активировались аденозином, в то время как члены семейства P2 в основном реагировали на АТФ, а метилксантины были над ними не властны.
В 1985 году Бёрнсток установил, что и P2-рецепторы можно поделить на два подсемейства — P2X и P2Y [13]. Было это сделано, опять же основываясь на их фармакологии и разной чувствительности к АТФ и его метиленовым производным.
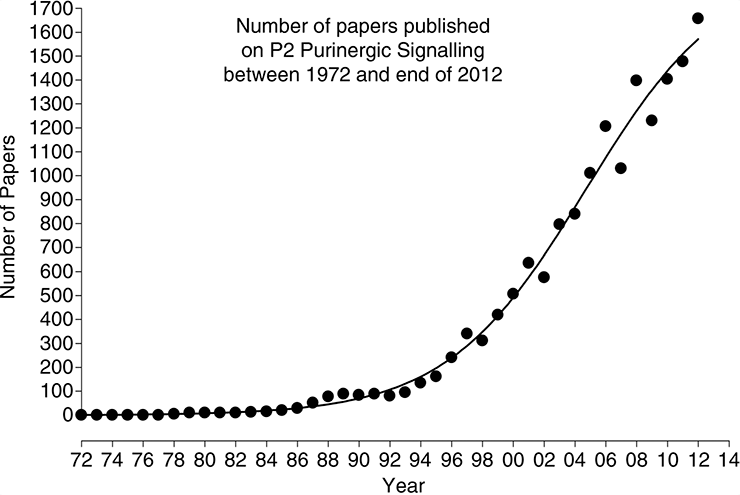
Однако развитие методик молекулярного клонирования [14], [15] в начале 90-х наконец приоткрыло завесу тайны над загадочными пуринорецепторами. Вначале были клонированы и охарактеризованы рецепторы P1, а потом дошла очередь и до P2. А дальше завертелось. Бёрнстоку окончательно поверили. «Пуримагическая гипотеза» потеряла свою магию и перестала быть гипотезой. Исследователи со всего мира бросились изучать новые рецепторы, а количество публикаций на тему «пуринергическая передача сигнала» начало расти буквально в геометрической прогрессии (рис. 8).
Рисунок 8. Количество работ, посвященных пуринергической передаче сигнала, в период с 1972 по 2012 год. Как видно из графика, начало 90-х стало переломным моментом в этой сфере исследований.
Также пуринергическую передачу сигнала стали называть «вторая жизнь», или «вторая